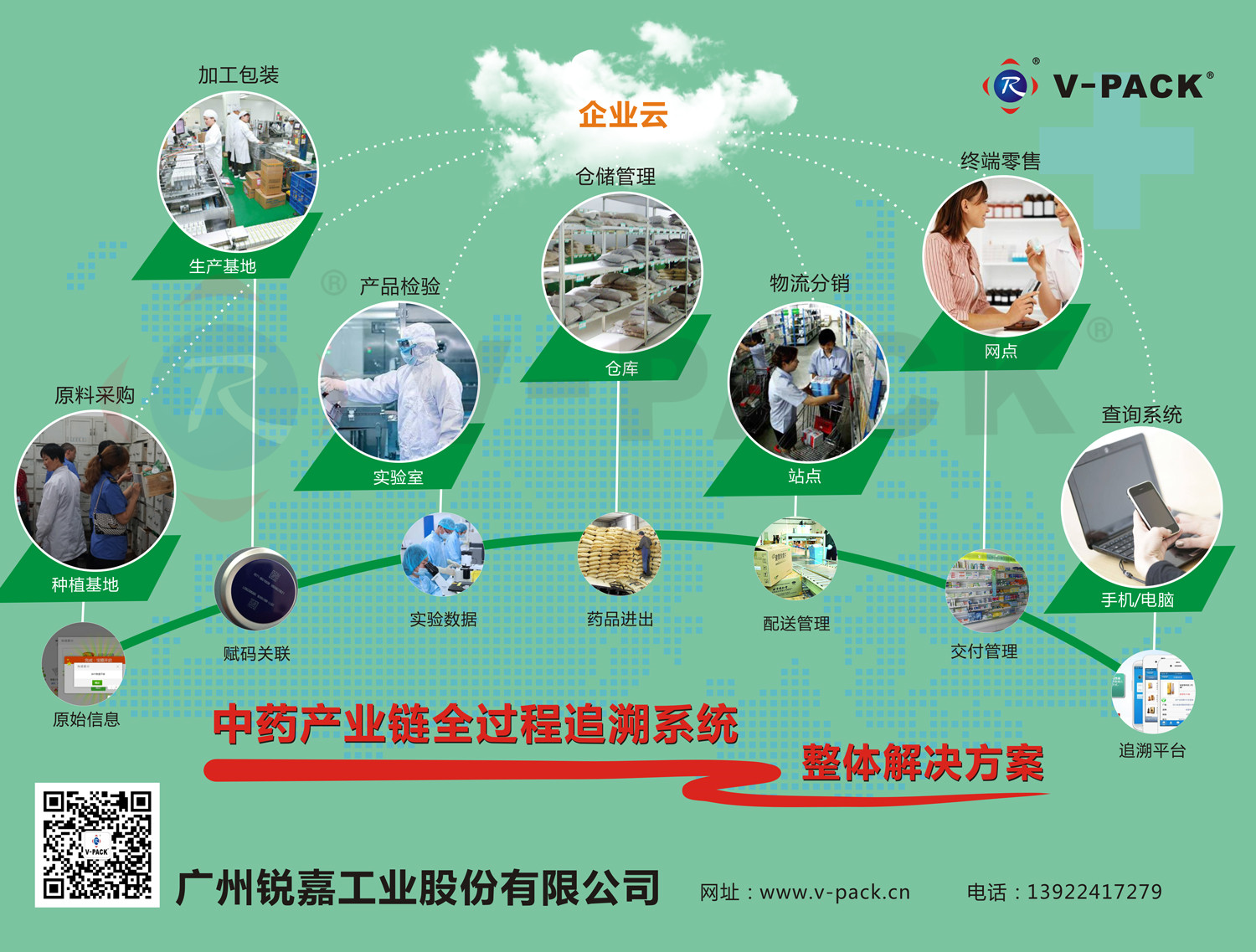
10个药品追溯标准发布实施,实现来源可查、去向可追
专栏:行业资讯
发布日期:2020-03-13
阅读量:3647
近日,国家药监局印发《药品上市许可持有人和生产企业追溯基本数据集》《药品经营企业追溯基本数据集》《药品使用单位追溯基本数据集》《药品追溯消费者查询基本数据集》《药品追溯数据交换基本技术要求》等5个标准。加上此前发布的《药品信息化追溯体系建设导则》等5个标准,截至目前,国家药监局组织编制的10个药品追溯标准规范现已全部发布实施。
为何要制定药品追溯标准规范?据了解,药品追溯标准规范是药品信息化追溯体系建设的重要组成部分,是强化追溯信息互通共享的重要基础。药品属于特殊商品,其质量安全关系到每个人的身体健康,因此加强药品来源可查、去向可追迫在眉睫。
其中,关于药品追溯、药品信息化追溯体系的概念需要理清。药品追溯是指通过记录和标识,正向追踪和逆向溯源药品的生产、流通和使用情况,获取药品全生命周期追溯信息的活动。
药品信息化追溯体系则是指药品上市许可持有人、生产企业、经营企业、使用单位、监管部门和社会参与方等,通过信息化手段,对药品生产、流通、使用等各环节的信息进行追踪、溯源的有机整体。
2018年5月,国家药监局启动药品追溯标准规范编制工作,明确药品信息化追溯体系建设总体要求,统一药品追溯码编码规则,提出药品追溯过程中需要企业记录、存储和提交信息的内容和格式,以及数据交换要求等。
另外,新修订的《疫苗管理法》明确提出,制定统一的疫苗追溯标准和规范;2019年12月落地实施的新版药品管理法,也明确要求应当制定统一的药品追溯标准和规范。
目前已发布的10个标准主要内容可分为药品追溯基础通用标准、疫苗追溯数据及交换标准、药品(不含疫苗)追溯数据及交换标准三大类。三大类标准既相互协调,又各有侧重。
基础通用标准
国家药监局从药品追溯统筹指导、夯实基础角度出发,提出了药品信息化追溯体系建设总体要求、药品追溯码编码要求和药品追溯系统基本技术要求,包括《药品信息化追溯体系建设导则》《药品追溯码编码要求》《药品追溯系统基本技术要求》等3个标准;
疫苗追溯数据及交换标准
据悉,考虑到疫苗单独立法的情况及其管理的特殊性,国家药监局从疫苗生产、流通到接种等环节,提出了追溯数据采集、存储及交换的具体要求,包括《疫苗追溯基本数据集》《疫苗追溯数据交换基本技术要求》等2个标准。
药品(不含疫苗)追溯数据及交换标准
国家药监局从药品(不含疫苗)生产、经营、使用和消费者查询等环节,提出了追溯数据采集、存储和交换的具体要求,包括《药品上市许可持有人和生产企业追溯基本数据集》《药品经营企业追溯基本数据集》《药品使用单位追溯基本数据集》《药品追溯消费者查询基本数据集》《药品追溯数据交换基本技术要求》等5个标准。
文章链接:制药网
为何要制定药品追溯标准规范?据了解,药品追溯标准规范是药品信息化追溯体系建设的重要组成部分,是强化追溯信息互通共享的重要基础。药品属于特殊商品,其质量安全关系到每个人的身体健康,因此加强药品来源可查、去向可追迫在眉睫。
其中,关于药品追溯、药品信息化追溯体系的概念需要理清。药品追溯是指通过记录和标识,正向追踪和逆向溯源药品的生产、流通和使用情况,获取药品全生命周期追溯信息的活动。
药品信息化追溯体系则是指药品上市许可持有人、生产企业、经营企业、使用单位、监管部门和社会参与方等,通过信息化手段,对药品生产、流通、使用等各环节的信息进行追踪、溯源的有机整体。
2018年5月,国家药监局启动药品追溯标准规范编制工作,明确药品信息化追溯体系建设总体要求,统一药品追溯码编码规则,提出药品追溯过程中需要企业记录、存储和提交信息的内容和格式,以及数据交换要求等。
另外,新修订的《疫苗管理法》明确提出,制定统一的疫苗追溯标准和规范;2019年12月落地实施的新版药品管理法,也明确要求应当制定统一的药品追溯标准和规范。
目前已发布的10个标准主要内容可分为药品追溯基础通用标准、疫苗追溯数据及交换标准、药品(不含疫苗)追溯数据及交换标准三大类。三大类标准既相互协调,又各有侧重。
基础通用标准
国家药监局从药品追溯统筹指导、夯实基础角度出发,提出了药品信息化追溯体系建设总体要求、药品追溯码编码要求和药品追溯系统基本技术要求,包括《药品信息化追溯体系建设导则》《药品追溯码编码要求》《药品追溯系统基本技术要求》等3个标准;
疫苗追溯数据及交换标准
据悉,考虑到疫苗单独立法的情况及其管理的特殊性,国家药监局从疫苗生产、流通到接种等环节,提出了追溯数据采集、存储及交换的具体要求,包括《疫苗追溯基本数据集》《疫苗追溯数据交换基本技术要求》等2个标准。
药品(不含疫苗)追溯数据及交换标准
国家药监局从药品(不含疫苗)生产、经营、使用和消费者查询等环节,提出了追溯数据采集、存储和交换的具体要求,包括《药品上市许可持有人和生产企业追溯基本数据集》《药品经营企业追溯基本数据集》《药品使用单位追溯基本数据集》《药品追溯消费者查询基本数据集》《药品追溯数据交换基本技术要求》等5个标准。
文章链接:制药网